Científicos desarrollan “carne” de hongo de laboratorio que podría ser una alternativa más barata al pollo
La textura y el sabor naturales de la proteína producida por el hongo se parecen mucho a los de la carne
Un grupo de científicos chinos modificó genéticamente un hongo para producir una “carne” rica en proteínas que, según afirman, podría convertirse en una alternativa económica y sostenible al pollo.
La ganadería, según diversos estudios, es responsable de aproximadamente el 14 % de las emisiones globales de gases de efecto invernadero. Además, requiere grandes extensiones de tierra y consume volúmenes significativos de agua dulce.
Si bien las proteínas cultivadas en laboratorio a partir de levaduras y hongos han surgido como posibles sustitutos de la carne convencional, uno de los principales desafíos ha sido procesarlas en productos que resulten atractivos para el consumidor.
Entre las opciones actuales, la proteína derivada del hongo Fusarium venenatum destaca por su textura y sabor naturales, muy similares a los de la carne de ave.
Aunque esta “carne” fúngica ya está aprobada para el consumo humano en países como Estados Unidos, Reino Unido y China, los científicos advierten que producir incluso pequeñas cantidades requiere una cantidad considerable de recursos.
Ahora, investigadores de la Universidad de Jiangnan han logrado mejorar significativamente su rendimiento. Al editar el genoma del Fusarium venenatum sin introducir ADN externo, optimizaron su eficiencia en la producción de proteínas y mejoraron su digestibilidad.
“Existe una fuerte demanda de proteínas mejores y más sostenibles para la alimentación”, señaló Xiao Liu, autor del estudio publicado en Trends in Biotechnology.
“Logramos que un hongo sea no solo más nutritivo, sino también más respetuoso con el medio ambiente al ajustar sus genes”, agregó.
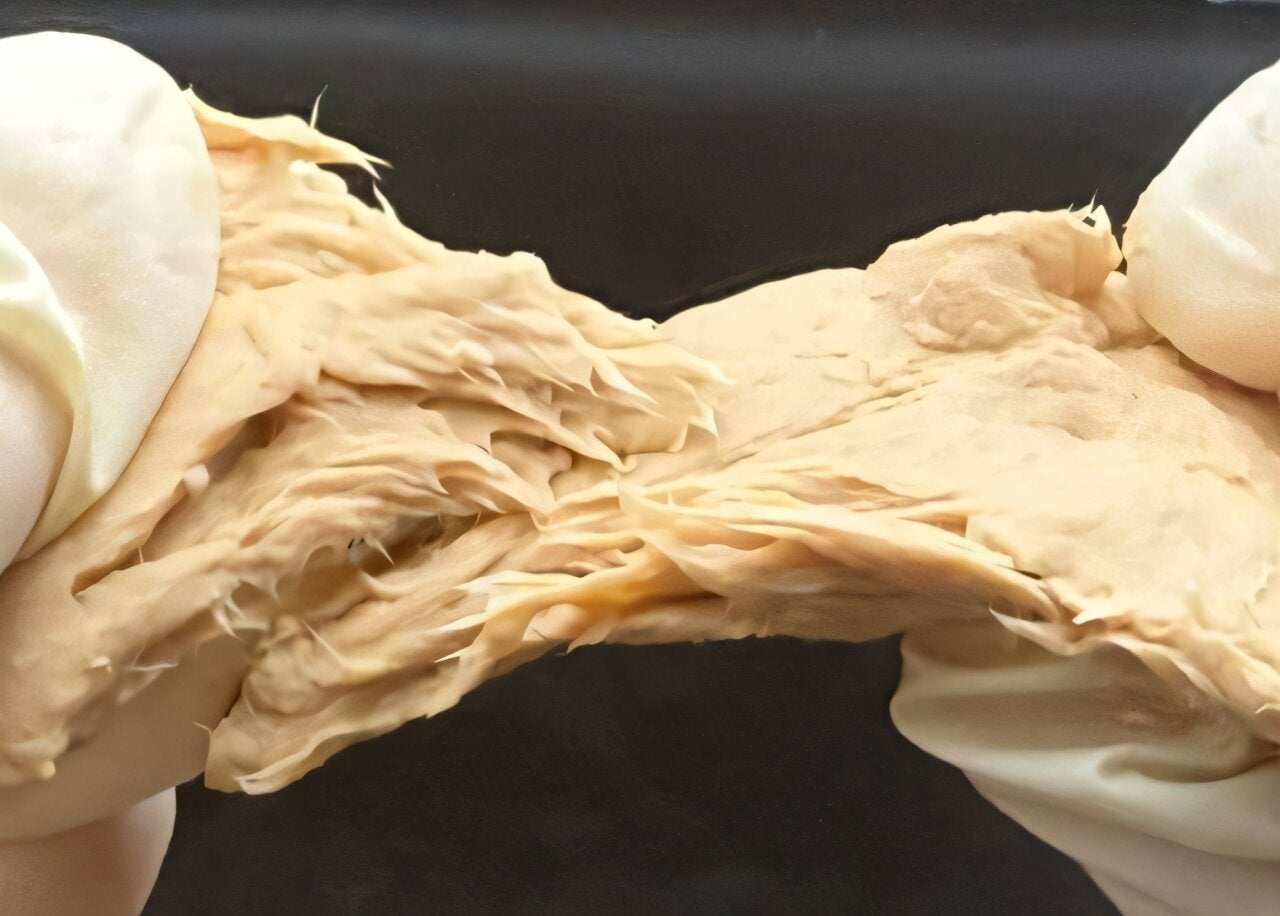
Los científicos eliminaron del ADN del hongo los genes asociados a dos de sus enzimas.
Uno de los cambios volvió más delgada la pared celular, lo que permitió almacenar una mayor cantidad de proteína en cada célula.
El otro modificó su metabolismo, reduciendo la necesidad de nutrientes para producir proteínas.
“Los alimentos editados genéticamente como este pueden responder a la creciente demanda sin los costos ambientales de la agricultura convencional”, señaló el Dr. Liu.
La cepa modificada del hongo, bautizada FCPD, necesitó un 44 % menos de azúcar para producir la misma cantidad de proteína que la cepa original, y lo hizo un 88 % más rápido, según el estudio.
Posteriormente, los investigadores simularon la producción de FCPD en seis países con distintas matrices energéticas. En comparación con la producción de pollo en China, concluyeron que la mioproteína derivada de FCPD requería un 70 % menos de tierra y reducía el riesgo de contaminación de agua dulce en un 78 %.
“Se puede concluir que una síntesis efectiva de mioproteína ofrece ventajas ambientales frente a la proteína animal y la carne cultivada”, señalaron los autores.
La modificación genética del hongo se realizó mediante CRISPR, una herramienta biotecnológica que permite editar de forma precisa el ADN de un organismo.
“Con políticas adecuadas para impulsar el desarrollo de la tecnología CRISPR en la agricultura celular y en la industria de proteínas alternativas, y con validaciones de seguridad más profundas, nuestra estrategia puede ampliarse a otros modelos de producción de proteínas alternativas”, concluyeron los investigadores.
Traducción de Leticia Zampedri








Bookmark popover
Removed from bookmarks