Regulador europeo revisa nuevo fármaco contra el coronavirus
La Agencia Europea de Medicamentos inicia un proceso de autorización acelerado para un fármaco de combinación de anticuerpos fabricado por AstraZeneca y destinado a prevenir el COVID-19
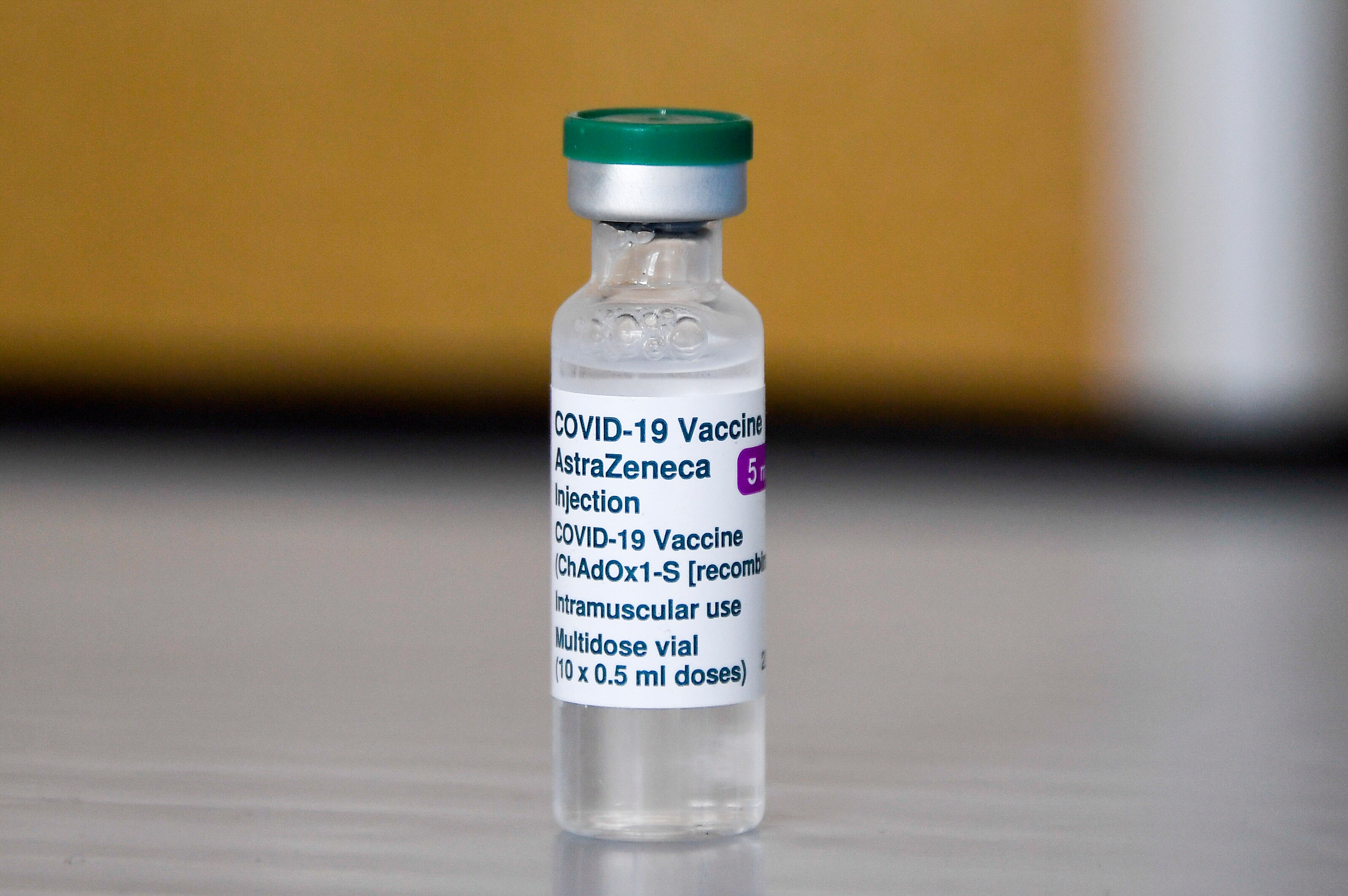
El regulador de medicamentos de la UE, la Agencia Europea de Medicamentos (EMA), informó el jueves en un comunicado que ha iniciado un proceso de autorización acelerado para un fármaco de combinación de anticuerpos fabricado por AstraZeneca y destinado a prevenir el COVID-19.
La EMA informó que comenzó a revisar datos preliminares de laboratorio y de investigación clínica para el fármaco Evusheld, una combinación de los dos anticuerpos monoclonales tixagevimab y cilgavimab. Los dos se adhieren a diferentes partes de la proteína de pico de coronavirus y están destinados a evitar que el virus infecte las células del cuerpo.
AstraZeneca pidió la semana pasada a la Administración de Alimentos y Medicamentos de Estados Unidos (FDA) que autorice el medicamento para uso de emergencia. Si se aprueba, sería el primer fármaco de este tipo al que se da luz verde para prevenir el COVID-19. Es probable que se limite a las personas con sistemas inmunitarios más débiles que no reciben suficiente protección sólo con la vacuna.
La investigación en fases finales mostró que la combinación de anticuerpos de AstraZeneca redujo en un 77% el riesgo de desarrollar síntomas de COVID-19 en personas que tenían el sistema inmunológico debilitado debido al cáncer, lupus u otras afecciones de salud.
Bookmark popover
Removed from bookmarks